Información Participantes
Healthy Medical Center SAS es un Centro de Investigación de estudios Clínicos, ubicado en la ciudad de Zipaquirá, Colombia, con amplia trayectoria y experiencia, lograda mediante la gestión en la Investigación Clínica desde el año 2012; cuenta con infraestructura, procesos y personal suficiente e idóneo para la conducción de ensayos clínicos de la Industria Farmacéutica.
Hemos participado en múltiples estudios clínicos en diversas áreas tales como Reumatología, Nefrología, Neumología, Endocrinologia y Cardiología. Esperamos proximamente desarrollar estudios en vacunas.
Si tienes alguna enfermedad crónica, te invitamos a que nos conozcas, podrías tener la oportunidad de participar en alguno de los estudios clínicos.
¿Qué es un Ensayo Clínico?

En un sentido amplio, y desde el punto de vista ético, es cualquier investigación realizada en humanos.
En general se trata de estudios en los que se compara, mediante medición de varios parámetros, los efectos de dos o más tratamientos o intervenciones terapéuticas en un grupo homogéneo de personas con una enfermedad o situación médica similar, con el objeto de detectar si uno de los tratamientos comparados es más o menos beneficioso que el otro.
Los ensayos clínicos surgen como la respuesta científica a la necesidad ética de garantizar la eficacia y la seguridad de los tratamientos que reciben los pacientes. Los ensayos clínicos proporcionan un método controlado, objetivo y reproducible para medir los efectos de un tratamiento sobre la salud, y así permiten establecer con objetividad una opinión sobre su utilidad en situaciones de enfermedad o prevención.
El ensayo clínico requiere un cuidado extremo porque su condición de experimentación le confiere una trascendencia ética, por implicar a seres humanos, y por la enorme repercusión que puede derivarse de sus resultados al poder éstos condicionar el tipo de tratamiento a recibir por miles de pacientes.
¿Cuáles son las fases de un Ensayo Clínico?
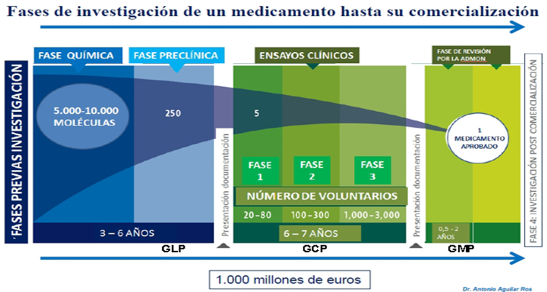
Al inicio, el descubrimiento de los medicamentos se dió de forma casual, pero en la actualidad es un proceso que implica reflexión, requiere de recompilación y análisis de datos, para finalmente tomar decisiones basadas en pruebas reales. En otras palabras, la investigación es una técnica refinada que se puede describir en 5 etapas.
Descubrimiento y Pre-Clínico
El primer paso en el proceso de descubrimiento de nuevos fármacos es identificar una necesidad médica no cubierta: ¿Qué sabemos de la enfermedad?, ¿Qué opciones terapéuticas existen, en caso de haber alguna?, ¿Cuentan los investigadores con la experiencia, la tecnología y los recursos económicos para resolver el problema?
El descubrimiento de un medicamento nuevo no es fácil, ya que se trata de un proceso largo y con una tasa de éxito muy baja. Aproximadamente, se estima que solo 250 de cada 10.000 moléculas de la etapa de investigación básica pasan a la fase de investigación preclínica.
En esta fase se ensaya exhaustivamente el compuesto seleccionado en el laboratorio para confirmar que será segura su administración en humanos. Concretamente, lo que se pretende es averiguar cómo se distribuye o elimina el medicamento del organismo y conocer sus efectos, a distintas dosis, en los órganos.
Fase I
En esta fase, que puede durar entre 6 meses y un año, se llevan a cabo los primeros estudios en seres humanos, que se hacen para demostrar la seguridad del compuesto y para guiar hacia la pauta de administración óptima en estudios posteriores.
En cada ensayo realizado en esta fase suelen participar entre 20 y 100 sujetos voluntarios sanos y/o pacientes.
Fase II
El objetivo de los ensayos que se realizan en esta fase es la búsqueda de dosis adecuadas y obtener los primeros datos sobre la efícacia del medicamento. En ellos participan entre 100 y 300 pacientes y son estudios terapéuticos exploratorios.
Fase III
Aquí, estos ensayos, que se llevan a cabo en mas de mil pacientes y que duran entre tres y seis años, evalúan la eficacia y seguridad del tratamiento experimental en condiciones de uso habituales y en comparación con los tratamientos ya disponibles para esa indicación concreta. Se trata de estudios terapéuticos de confirmación. Los resultados obtenidos en los estudios llevados a cabo en la Fase III proporcionan la base para la aprobación del fármaco.
Fase IV o Fase de Aprobación y Registro
En esta fase se lleva a cabo la solicitud, a las agencias reguladoras competentes, de la autorización para la comercialización del fármaco. El informe, que puede llegar a tener mas de 120.000 páginas, ha de contener toda la información recopilada a lo largo de todo el proceso de investigación y desarrollo del medicamento y debe demostrar que el nuevo fármaco tendrá el efecto deseado.
Para ver el articulo completo se puede dirigir al siguiente link: https://www.msdsalud.es/Assets/docs/dossier_msd/proceso-aprobacion-farmaco.pdf
¿Cuáles son los beneficios de un Ensayo Clínico?

- Obtener acceso a nuevos y posibles medicamentos efectivos disponibles solo para las personas que participan en el ensayo.
- Obtener atención médica dirigida a una enfermedad o condición de salud particular.
- Obtener mayor información sobre su enfermedad y estado de salud.
- Tener la oportunidad de ayudar a la sociedad y otras personas que comparten su enfermedad o condición de salud, contribuyendo a la investigación médica.
- Al participar usted está contribuyendo al desarrollo de nuevos medicamentos, contribuye al descubrimiento de formas de prevenir o curar enfermedades o condiciones de salud
Entre las desventajas o riesgos se encuentran:
- Análisis y consultas médicas mas frecuentes
- Es posible que el medicamento en estudio no le haga sentir mejor.
- En casos muy raros se pueden presentar efectos adversos.
¿Qué debo saber como participante de un Ensayo Clínico?

Todo estudio clínico tiene como objetivo principal averiguar la eficacia del medicamento en estudio lo cual permitiría a los pacientes una vida mas longeva mejorando el funcionamiento físico y brindando una mayor calidad de vida.
La participación en estos estudios es completamente voluntaria, la persona decide si quiere hacer parte del estudio, y en caso de participar, la persona puede dejar el estudio en cualquier momento.
El participante tiene derecho a comprender el por qué se está realizando el estudio y qué sucederá en caso que decida participar. El participante tiene derecho a hacer todas las preguntas que tenga sobre el estudio en el cual colabora y a recibir respuestas satisfactorias a sus preguntas.
Durante la participación en el estudio, generalmente el patrocinador cubre con los gastos de transporte, así como el costo de exámenes, asistencia médica y reembolsará cualquier gasto razonable relacionada a la participación del estudio.
La persona que participa puede estar tranquilo en cuanto a la confidencialidad de sus datos personales o la información recopilada (ej. registros médicos) en relación con el estudio que se esté llevando a cabo. Sus datos se tratarán de manera estrictamente confidencial y su identidad no se revelará en publicaciones ni informes generados a partir del estudio en el cual participa.
También es importante tener en cuenta que el participante es responsable de seguir las indicaciones del médico del estudio, así como de su personal del estudio. Recuerde que su colaboración va en pro de un bien que trasciende lo personal.
Cualquier persona tiene derecho a consultar toda la información del estudio a través de la pagina web www.clinicaltrials.gov ya que esta pagina se encuentran registrados todos los estudios clínicos que se están desarrollando a nivel mundial.